CONTROLE DE QUALIDADE NO LABORATÓRIO DE ANÁLISES CLÍNICAS: UMA REVISÃO
Fernando Pedrosa Coelho
Artigo Científico Apresentado à Universidade Candido Mendes - UCAM, como requisito parcial para a obtenção do título de Especialista em Análises Clínicas e Microbiologia.
RESUMO
Este estudo teve como preocupação principal o controle de qualidade no laboratório de análises clínicas, buscando evitar erros e assegurar maior confiabilidade nos laudos liberados. O objetivo principal deste estudo foi descrever as etapas do processo de controle de qualidade no laboratório de análises clínicas. Foi empregado como metodologia a pesquisa bibliográfica de artigos, monografias, dissertação, e outros documentos publicados nas bases de dados do Scielo, Lislacs, Google acadêmico e periódicos. A implantação correta de um controle da qualidade garante ao cliente um serviço de saúde eficaz e contribui para o diagnóstico médico. Em contrapartida, um controle de baixa qualidade pode levar a diagnósticos errados. As fases do controle de qualidade são as fases pré-analítica, analítica e pós-analítica. Programas como PNCQ ajuda os laboratórios a melhorar o controle de qualidade através de ensaios de proficiência e ferramentas. Com a qualidade aumentada o laboratório passa a oferecer serviços com mais seguranças e qualidade. O controle de qualidade no laboratório de análises clínicas é muito importante para o paciente, médico e para o próprio laboratório e a implementação do PNCQ constitui uma alternativa para melhorar a qualidade dos serviços prestados pelo laboratório.
Palavras-chave: Laboratório. Qualidade. Gestão da qualidade em saúde.
ABSTRACT
This study had as main concern the quality control in the laboratory of clinical analyzes, seeking to avoid errors and to assure greater reliability in the released reports. The main objective of this study was to describe the steps of the quality control process in the laboratory of clinical analyzes. The bibliographical research of articles, monographs, dissertation, and other documents published in Scielo, Lislacs, Google academic and periodical databases was used as methodology. The correct implementation of a quality control guarantees the client an effective health service and contributes to the medical diagnosis. In contrast, poor quality control can lead to misdiagnosis. The phases of quality control are the pre-analytical, analytical and post-analytical phases. Programs such as PNCQ help laboratories improve quality control through proficiency testing and tools. With increased quality, the laboratory offers services with more security and quality. Quality control in the clinical analysis laboratory is very important for the patient, doctor and the laboratory itself, and the PNCQ implementation is an alternative to improve the quality of the services provided by the laboratory.
Keywords: Laboratory. Quality. Quality management in health.
Introdução
O presente estudo tem como tema o controle de qualidade no laboratório de análises clínicas, buscando principalmente evitar os possíveis erros nos exames laboratoriais, assegurando maior confiabilidade nos laudos laboratoriais e possibilitando que o médico possa estabelecer de forma correta o diagnóstico, tratar, prevenir ou curar determinada patologia.
Assim, construiu-se os seguintes questionamentos:
- Qual a importância do controle de qualidade para o laboratório de análises clínicas?
- Quais as consequências de um controle da qualidade inadequado?
- Quais são as etapas desse processo?
- O que é o Programa Nacional de Controle da Qualidade (PNCQ)?
Com o grande crescimento de laboratórios de análises clínicas no Brasil nos últimos anos, torna-se de fundamental importância laudos liberados com maior fidedignidade. Além disso, nos últimos anos a maior causa de reivindicações judiciais nos Estado Unidos tem sido por causa dos erros nos diagnósticos. (SANTOS; ZANUSSO JUNIOR, 2015). Um resultado errado prejudica o diagnóstico de uma patologia e do tratamento correto do paciente (MORITA, 2010 apud SILVA, 2017). Portanto, o controle da qualidade se torna uma ferramenta fundamental nesse processo (BARBOZA, 2011 apud SILVA, 2017).
De acordo com Santos e Zanusso Junior (2015, p.60),
O exame laboratorial é um instrumento que permite ao médico diminuir as dúvidas e estabelecer um diagnostico com precisão. A padronização e a realização do controle de qualidade nos laboratórios clínicos representam elementos imprescindíveis para a rotina laboratorial. Uma analise laboratorial bem realizada contribui para a preservação ou restauração da saúde do paciente, agregando elevado valor a assistência médica, otimizando a qualidade do serviço prestado.
Dentro deste contexto, o objetivo principal deste estudo foi descrever as etapas do processo de controle de qualidade no laboratório de análises clínicas.
Para alcançar o objetivo proposto, foi empregado como metodologia a pesquisa bibliográfica de artigos, monografias, dissertação, e outros documentos publicados nas bases de dados do Scielo, Lislacs, Google acadêmico, periódicos.
Desenvolvimento
A melhora contínua passou a ser objetivo de toda organização e instituição, inclusive dos laboratórios de análises clínicas. Estes devem assegurar os resultados de modo fidedigno e consistente, possibilitando que a informação contida no laudo laboratorial reflita o diagnóstico correto do paciente. Assim, torna-se necessário a melhoria continuamente desse processo, a fim de evitar o mínimo possível de erro durante as análises (CHAVES, 2010).
O controle de qualidade são operações e técnicas usadas para monitorar o processo e certificar de que o resultado se encontra dentro do padrão exigido (BRASIL, 2005). O controle de qualidade pode ainda ser dividido em controle externo e controle interno (LOPES, 2010 apud MARTELLI, 2011).
O controle externo da qualidade (CEQ) pode ser definido como uma atividade que usa sistemas de ensaios de proficiência, análise de padrões certificados e comparações interlaboratoriais para avaliar o desempenho dos sistemas analíticos. Já o controle interno da qualidade (CIQ) se refere a procedimentos realizados junto com as amostras de exame do paciente para verificar se o sistema analítico se encontra dentro do limite estabelecido (BRASIL, 2005).
No laboratório de análises clínicas, a garantia da qualidade é obtida a partir do controle de todas as etapas que norteiam o processo, sendo elas: fase pré-analítica (CEQ), fase analítica e fase pós-analítica (CIQ) (CHAVES, 2010).
A fase pré-analítica inicia-se com “o pedido do exame pelo médico”. Nesta primeira etapa o médico escolhe os exames laboratoriais adequados para o diagnóstico do paciente a partir de seu conhecimento e levando em conta o que foi relatado na consulta pelo paciente (GOLDSCHMIDT, 1999; GOLDSCHMIDT, 2002 apud GUIMARÃES et al., 2011).
A segunda etapa da fase pré-analítica compreende a “obtenção de informações do paciente” corresponde a uma anamnese feita pelo atendente que irá obter dados do paciente como idade, gênero, posição do corpo, atividade física, jejum, dieta, uso de medicamentos, alcoolismo, tabagismo, uso de drogas. Além disso, o atendente também deve dar instruções ao paciente para o dia da coleta (BRASIL 2005a; SPBC, 2009; LIPPI et al., 2006 apud GUIMARÃES et al., 2011).
A etapa seguinte consiste da “coleta e identificação da amostra biológica”. Após a preparação do paciente e coleta de dados, inicia-se a coleta da amostra pelo técnico de laboratório ou bioquímico (BRASIL 2005a; SPBC, 2009; LIPPI et al., 2006 apud GUIMARÃES et al., 2011).
Após a coleta, a amostra é identificada, caso a amostra seja traga de casa pelo paciente, como no caso de fezes ou urina, a mesma e identificada pelo técnico ou bioquímico no ato da entrega no laboratório. Estas identificações devem conter o nome do paciente, o número de registro para rastreio e o nome do responsável pela coleta (BRASIL, 2005a; JOINT COMMISSION INTERNATIONAL, 2007; WORLD HEALTH ORGANIZATION, 2007; LIPPI, 2008 apud GUIMARÃES et al., 2011).
A próxima etapa consiste no “Transporte e armazenamento” das amostras. O transporte deve ser feito em recipiente adequado, higienizável e isotérmico (quando necessário), a fim de manter as amostras estáveis até a sua análise (BRASIL, 2002 apud GUIMARÃES et al., 2011). O recipiente deve conter também simbologia de risco biológico com os dizeres “Espécimes para Diagnóstico” e com o logo do laboratório (BRASIL, 2005).
A última etapa da fase pré - analítica consiste no “recebimento, critérios de rejeição e aceitação das amostras e rastreabilidade dos processos” (GUIMARÃES et al., 2011). As amostras são recebidas pelo analista e mediante os critérios do laboratório as amostras são aceitas ou não. Nesta etapa também pode ser necessário rastrear processos anteriores que tenham acontecido durante a coleta ou recebimento das amostras. (BRASIL, 2005; ASSOCIAÇÃO MERCOSUL DE NORMATIZAÇÃO, 2009 apud GUIMARÃES et al. 2011).
Segundo Silva (2017) e Guimarães et al. (2011) a fase pré-analítica tem maiores chances de erros em relação as demais fases do controle de qualidade.
Conforme Lopes (2011) citado por Silva (2017, p.18), “a fase pré-analítica é a fase mais suscetível aos erros, isso porque todos os processos que envolvem essa fase são realizados fora do laboratório clínico e estão diretamente ligadas a tarefas manuais”.
A fase analítica
A fase analítica ou a fase de realização do exame constitui um conjunto de procedimentos realizados durante o exame do paciente e tem como objetivo garantir que o processo esteja dentro dos padrões estabelecidos (OLIVEIRA; MENDES, 2010 apud SANTOS; ZANUSSO JUNIOR, 2015). Para esta fase o controle interno de qualidade do laboratório deve dispor de instruções escritas, atualizadas e disponíveis para todos os processos, podendo ser utilizadas instruções do fabricante (BRASIL, 2005).
Nesta etapa as amostras – controle (amostras com valor conhecido) devem ser analisadas todos os dias, a fim de assegurar a precisão nos ensaios realizados. Essas amostras controles quando analisadas junto com as amostras do paciente permite analisar o desempenho do processo analítico. (SCHMITZ et al., 2008 apud SANTOS; ZANUSSO JUNIOR, 2015)
Fase pós – analítica
É a última etapa após o exame laboratorial (fase analítica). Nesta fase ocorre a validação e, em seguida a liberação do laudo laboratorial. Este laudo será entregue ao paciente que deverá encaminhar ao médico, que por sua vez, tomará a decisão para o tratamento do paciente. Estes laudos são confidenciais e o laboratório deve manter os laudos arquivados por cinco anos. (LOPES, 2003 apud SANTOS; ZANUSSO JUNIOR, 2015).
Como as outras duas fases é uma fase de extrema importância, pois qualquer erro que ocorra em uma das fases anteriores pode comprometer o relatório final, levando o laboratório a ser desacreditado e podendo levar o paciente a um diagnóstico errado (BANFI, 2003; MOTTA, 2009; POP, 2011 apud COSTA; MORELI, 2012).
Abaixo está uma tabela que demonstra os maiores erros encontrados nas fases pré-analítica, analítica e pós-analítica:
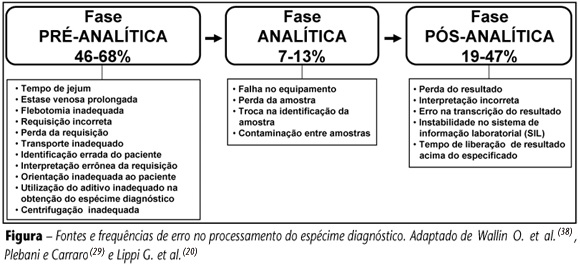
Como podemos ver as fases com maiores índicies de erros são a fase pré- analítica e pós-analítica.
Conforme Plebani et al. (2006) citado por Vieira et al. (2011, p.205),
Estima-se entre 46% e 68% o percentual de erros laboratoriais referentes a problemas ocorridos durante a fase pré-analítica (...). Os erros frequentemente associados à fase pós - analítica correspondem às falhas na liberação dos resultados, por erros de transcrição ou digitação ou pelo não cumprimento do prazo de entrega.
Para evitar esses erros surgiu no Brasil, por volta de 1979, o Programa Nacional de Controle de qualidade (PNCQ). O PNCQ é um provedor de proficiência para os exames realizados no laboratório de análises clínicas. De acordo com este programa,o laboratório clínico deve participar de ensaios de proficiência para todos os exames realizados na sua rotina. O PNCQ tem como os objetivos principais:
· Divulgar e implantar em todo o Território Nacional o Programa de Controle Externo da Qualidade - PRO-EX ou Ensaio de Proficiência, destinado aos Laboratórios Clínicos e Bancos de Sangue, monitorando seu desempenho analítico;
· Obedecer às normas e diretrizes internacionais preconizadas pelos organismos nacionais e internacionais no planejamento, composição, implantação e avaliação, relativos aos ensaios de proficiência;
· Elaborar apostilas sobre assuntos técnico-científicos, administrativos ou de controle da qualidade para auxiliar o Laboratório Participante na sua educação continuada;
· Avaliar os resultados dos seus Participantes, calculando a média de consenso, desvio-padrão, coeficiente de variação e desvio relativo à média, assim como, a avaliação mensal e anual, fornecendo-lhes um conceito e classificação;
· Incentivar e auxiliar os Laboratórios Participantes a preparar os procedimentos para a implantação de um sistema de gestão da qualidade, compatível com o seu porte e complexidade. (PNCQ, 2017)
Em 2009, o PNCQ lançou programa chamado PNCQ Gestor, que se trata de uma ferramenta com a função de ajudar os laboratórios a cumprir com os requisitos da RDC 302/2005 da ANVISA. O PNCQ Gestor conta com um manual de instruções e um "pen drive" com modelos de formulários, procedimentos de qualidade, instruções de trabalho, descrição de cargos, manual da qualidade entre outros (PNCQ, 2017). Sem programas como este o laboratório não possui métodos para avaliar a exatidão do seu trabalho (MARTELLI, 2011).
Conclusão
Conclui-se que a implantação correta de um controle da qualidade garante ao cliente um serviço de saúde eficaz e também contribui para o diagnóstico médico. Em contrapartida, um controle de baixa qualidade pode levar a diagnósticos errados, e tratamentos inadequados, além de reduzir a “imagem” do laboratório de análises clínicas.
As etapas do controle de qualidade são: fase pré-analítica, fase analítica e fase pós-analítica, sendo a primeira a que mais se encontra possibilidade de erros, pois a maioria dos seus procedimentos é realizado por pessoas que estão consequentemente sujeitas a erros. Em seguida a fase pós-analítica que também tem grande índices de erros.
Sendo assim torna-se necessário a implementação de programas recomendados pela ANVISA como o PNCQ, que visam melhorar a qualidade dos serviços prestados pelo laboratório, através de ensaios de proficiência e monitoramento. Com a qualidade melhorada, o laboratório passa a fornecer serviços de saúde com eficácia, e podendo assim reduzir o seu custo e aumentar sua produtividade.
REFERÊNCIAS
BERLITZ, Fernando de Almeida. Controle da qualidade no laboratório clínico: alinhando melhoria de processos, confiabilidade e segurança do paciente. J. Bras. Patol. Med. Lab., Rio de Janeiro , v. 46, n. 5, p. 353-363, Oct. 2010. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442010000500003&lng=en&nrm=iso>. Acesso em: 12 de junho de 2017.
BRASIL. Ministério da Saúde. Resolução RDC nº302, de 13 de Outubro de 2005. Diário Oficial da União de 14 de outubro de 2005. Disponível em: <http://portal.anvisa.gov.br/documents/10181/2718376/RDC_302_2005_COMP.pdf/7038e853-afae-4729-948b-ef6eb3931b19> Acesso em: 18 de julho de 2017.
CHAVES, Carla D. Controle de qualidade no laboratório de análises clínicas. J. Bras. Patol. Med. Lab., Rio de Janeiro , v. 46, n. 5, p. 352, Oct. 2010. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442010000500002&lng=en&nrm=iso>. Acesso em: 12 de junho de 2017.
CHAVES, Josefa Sieira Caamaño; MARIN, Victor Augustus. Avaliação do controle externo da qualidade nos laboratórios clínicos do Rio de Janeiro de 2006 a 2008. J. Bras. Patol. Med. Lab., Rio de Janeiro, v. 46, n. 5, p. 391-394, Oct. 2010. Disponível em:< http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442010000500008&lng=en&nrm=iso>. Acesso em: 12 Junho 2017.
CORREIA e SILVA, Maria Patrícia Brito de. Qualidade na etapa pré-analítica de um laboratório de análise clínica. 2017. Monografia (Conclusão do curso) - Instituto Nacional de Ensino Superior e Pesquisa Centro de Capacitação Educacional, Recife. Disponível em:<http://www.ccecursos.com.br/img/resumos/qualidade-na-etapa-pr--anal-tica-de-um-laborat-rio-de-an-lise-cl-nica.pdf>Acesso em: 13 de julho de 2017.
COSTA, Vivaldo Gomes da; MORELI, Marcos Lázaro. Principais parâmetros biológicos avaliados em erros na fase pré-analítica de laboratórios clínicos: revisão sistemática. J. Bras. Patol. Med. Lab., Rio de Janeiro , v. 48, n. 3, p. 163-168, jun. 2012 . Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S167624442012000300003&lng=pt&nrm=iso>. Acesso em: 19 de julho de 2017.
FERNANDES, Cristiane F. Oliveira; Talma R. L.. Analysis of the pre-analytical phase in a private pathology laboratory of Maringá city-PR, Brazil. J. Bras. Patol. Med. Lab., Rio de Janeiro , v. 52, n. 2, p. 78-83, Apr. 2016 . Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442016000200078&lng=en&nrm=iso>. Acesso em 17 de Junho de 2017.
GUIMARÃES, Alexandre Costa et al. O Laboratório Clínico e os Erros Pré-Analíticos. Clinical & Biomedical Research, [S.l.], v. 31, n. 1, apr. 2011. ISSN 2357-9730. Disponível em: <http://www.seer.ufrgs.br/index.php/hcpa/article/view/13899/11507>. Acesso em: 16 de Junho de 2017.
MARTELLI, Anderson. Gestão da Qualidade em Laboratórios de Análises Clínicas UNOPAR Cient Ciênc Biol Saúde 2011; 13(Esp):363-8. Disponível em: <file:///C:/Users/Seven/Downloads/1097-4243-1-PB%20(1). pdf>. Acesso em 17 de Junho de 2017.
PNCQ. Programa Nacional de Controle de Qualidade. Objetivos. Disponível em:< https://www.pncq.org.br/Noticia/BR/Index/4 >Acesso em: 13 de julho de 2017.
SANTOS, Adriano Palhari dos; ZANUSSO JUNIOR, Gerson. Controle de qualidade em laboratórios clínicos. Revista Uningá, Paraná, v.45, p.60-67, jul./set. 2015. Disponível em: <http://www.mastereditora.com.br/periodico/20150924_075713.pdf>. Acesso em 17 de junho de 2017.
VIEIRA, Keila Furtado et al . A utilidade dos indicadores da qualidade no gerenciamento de laboratórios clínicos. J. Bras. Patol. Med. Lab., Rio de Janeiro, v. 47, n. 3, p. 201-210, June 2011. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442011000300002&lng=en&nrm=iso>. Acesso em 17 de junho de 2017.



